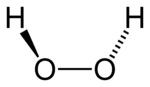
Peroxid vodíku
Peroxid vodíku (H2O2) (triviálně kysličník) je čirá kapalina, o něco viskóznější než voda. Patří mezi hydroxykyseliny. Má silné oxidační, ale i redukční vlastnosti a často se používá jako dezinfekce (3% vodný roztok). Rovněž se často využívají jeho bělící účinky při odbarvování vlasů, v ponorkách je částí pohonného média torpéd. Během druhé světové války byl používán jako raketovépalivo ať už samostatně – jako jednosložkové palivo, tj. katalytickým rozkladem na paroplyn (nejznámější motory Hellmutha Waltera, popřípadě z pozdější doby "raketový pás - rocket belt" z bondovek), nebo ve spojení s etylakoholem (lihem), hydrazinem nebo petrolejem (kerosenem). Při použítí s hydrazinhydrátem má samozápalné účinky - tj při smísení obou látek dojde k okamžitému samovznícení.
Po válce se od použití peroxidu jako okysličovadla až na pár výjimek (Black Arrow) ustoupilo a místo toho se používá oxid dusičitý, který je ovšem prudce jedovatý. Naproti tomu katalytický rozklad peroxidu na paroplyn se jako pomocný zdroj v raketové technice používá od A4 (známější jako V-2) až po RD 107/108, což jsou hlavní motory prvního a druhého stupně ruskérakety R-7, v současnosti známé ve své nejvýkonnější verzi jako Sojuz U.
V současnosti se uvažuje o návratu k peroxidu především z ekologických důvodů. Peroxid vodíku je silnější kyselina než voda, poskytuje soli hydrogenperoxidy (HO2)- a peroxidy (O2)2-
Poprvé byl peroxid vodíku připraven v roce 1818L. J. Thénardem reakcí kyseliny sírové s peroxidem barnatým a odpařením nadbytečné vody za sníženého tlaku dle rovnice:
BaO2 + H2SO4 → H2O2 + BaSO4
Nejdůležitější z peroxidů a výchozí složkou výše uvedené reakce je BaO2, vznikající při zahřívání BaO v kyslíkové atmosféře.
Na 2-alkylantrachinon se působí vodíkem v přítomnosti katalyzátoru za vzniku 2-alkylantrachinolu. Zaváděním vzduchu se uvolňuje peroxid vodíku a zpět vzniká výchozí látka.
Rozklad: 2H2O2 → 2H2O + O2
Rozklad zpomaluje např. močovina, kyselina fosforečná; naopak jej urychluje oxid manganičitý, manganistan draselný, jodid draselný, stříbro nebo platina.
Reakcí s acetonem vzniká třaskavá sloučenina s názvem peroxoaceton.
Přeměna na disulfan: H2O2 + 2 H2S → H2S2 + 2 H2O